La piel del recién nacido (RN) posee los elementos anatómicos y fisiológicos para adaptarse al medioambiente y realizar funciones esenciales para mantener el equilibrio electrolítico, regular la temperatura corporal, secretar hormonas, protegerse de la radiación solar, y prevenir infecciones.1 Sin embargo, durante el primer año de vida, la piel enfrenta un proceso de maduración para alcanzar características similares a las de la piel adulta, en términos de composición, estructura y función.1
La epidermis del RN es 30% más delgada, debido a un menor número de capas en el estrato córneo (EC), lo que facilita la penetración de sustancias potencialmente tóxicas.2 Los corneócitos y queratinocitos son de menor tamaño y producen cantidades insuficientes de factores de hidratación natural (NMF, por sus siglas en inglés); esto resulta en bajos valores de hidratación de la piel.1 Además, la pérdida de agua transepidérmica (TEWL, en inglés) varía entre 4–10g/m2/h, ya que algunos factores (edad gestacional por debajo de las 37 semanas, temperatura ambiente superior a 25°C, o sudor en regiones anatómicas, como planta del pie, palma de la mano y antebrazos) pueden aumentar estos valores.1
También, el potencial de concentración de hidrógeno (pH) de la piel del RN puede tener valores entre 6,0 y 7,5, y adquirir acidez entre el tercer y cuarto día de vida, pero estabilizarse durante los primeros tres meses de vida, con valores entre 4,5 y 5,53,4 (considerados los valores fisiológicos de pH para la piel). El pH es una escala que permite medir el nivel de acidez, neutralidad o alcalinidad de una solución o superficie. La escala abarca valores de 1,0 a 14,0 (7 es considerado neutro; un valor menor que 6,9 es considerado ácido; y uno mayor que 7,1 es básico o alcalino). Los valores más cercanos a 1,0 son más ácidos, mientras que los más cercanos a 14,0 son considerados más básicos.5 Por eso, es necesario establecer cuidados específicos en cuanto a la selección de productos de higiene adecuados para el RN, con el fin de preservar la integridad y promover la madurez de la piel.6
El primer baño del RN es realizado por profesionales de la salud y cuidadores, no sólo para eliminar sustancias como saliva, orina, heces, suciedad, grasa y microorganismos que se adhieren a la capa externa de la piel, sino también para promover su desarrollo y confort.7 El baño puede ser realizado con agua o con un producto de limpieza, como el jabón líquido o en barra.7
Los jabones en barra son uno de los productos de limpieza más antiguos. Su composición química ha evolucionado a lo largo de los años. Actualmente, se destacan algunos tipos de jabones en barra que se usan para la higiene de la piel:
- Tradicional: deriva del proceso de reacción entre un álcali y glicéridos de origen animal o vegetal que, de acuerdo con la proporción de ingredientes, puede aumentar o reducir la capacidad de eliminar los lípidos del EC.8 Su valor de pH es comúnmente alcalino (entre 9 y 11)8 y, en combinación con el agua, promueve el aumento del pH de la piel por encima de 8,0, ya que pasa por una reacción de hidrólisis y libera el álcali sobre la piel9
- Transparente o semitransparente: tiene valores de pH menos alcalinos (entre 8 y 10) debido a su neutralización con aminas alcalinas ligeras, como la trietanolamina, que mejoran la suavidad del producto.8 Puede contener glicerina (concentración variada) para evitar la cristalización y opacificación del producto, y mejorar la hidratación de la piel9
- Syndet: mezcla tensioactivos sintéticos, obtenidos por procesos químicos diferentes a la saponificación. Suelen tener pH cercanos a los de la piel8
- Combinado: combina el jabón en barra tradicional (con tensioactivos aniónicos suaves, como isotionato y sulfosuccinato de sodio) y el syndet. Tiene un valor de pH entre 5,0 y 7,58
- Antibacterianos: poseen una composición similar al jabón en barra tradicional, con uno o más ingredientes antibacterianos. Dependiendo de los ingredientes y de su concentración, pueden ser considerados medicamentos o cosméticos según la lesgislación del país. Su uso ha sido limitado en algunos países debido a la ausencia de estudios que comprueben su eficacia. Su pH es generalmente alcalino, con valores mayores a 8.8
Tanto los jabones syndet como los combinados proporcionan una limpieza adecuada, pero con menor eliminación del manto hidrolipídico. Suelen causar menor irritación de la piel.8
Los jabones líquidos, por su parte, están compuestos de tensioactivos sintéticos en una dispersión acuosa. Su valor de pH puede variar entre 5,5 y 7,0, o sea, levemente acidificado a neutro.8 Los tensioactivos son sustancias de origen natural o sintético, formadas por una porción de la molécula hidrofílica que interactúa con el agua (fase hidrofílica) y otra parte lipofílica que actúa sobre la grasa, el sebo o la suciedad de la piel, y microorganismos (parte lipofílica).8 Según su carga, existen tres tipos de tensioactivos: aniónicos, anfóteros y no iónicos.8 Diferentes tipos de tensioactivos se pueden combinar en el mismo producto (por ejemplo, anfótero y aniónico) para desarrollar jabones más suaves para la piel, es decir, más seguros y con menor interacción con la fisiología cutánea.7 Además, pueden elaborarse jabones líquidos en combo, es decir, combinaciones de syndet (tensioactivos) con ingredientes de un jabón en barra tradicional. Sin embargo, dependiendo de la proporción de ingredientes utilizados y el efecto de los tensioactivos en la piel, puede haber un aumento en el pH y una alteración de los procesos homeostáticos de la barrera cutánea.4
Tensioactivos aniónicos, anfóteros y no iónicos
Los tensioactivos aniónicos están cargados negativamente en su parte hidrofílica y, por lo tanto, en contacto con el agua, liberan uno o más iones negativos.10 Son tensioactivos de uso común en las formulaciones, porque generan espuma y promueven una buena limpieza.10 Según el grupo polar, se clasifican en: sulfonato, sulfatado, carboxilado y fosfatado. Dependiendo de su estructura química, cantidad e interacción con otras sustancias, pueden tener una acción variable con la piel, lo que proporciona mayor o menor suavidad. Por ejemplo, los tensioactivos sulfatados, como Sodium lauryl sulfate y Ammonium lauryl sulfate, pueden causar una mayor irritación de la piel debido a la mayor acción desengrasante y desnaturalización de las proteínas del EC, lo que provoca un desequilibrio en el manto hidrolipídico, hasta su regeneración.10,11 Además, el tensioactivo carboxilado de hidróxido de sodio presente en el jabón en barra tradicional puede generar una mayor irritación en la piel, debido a la liberación de álcali y un aumento en su valor de pH.10,11 Sin embargo, en el grupo de los sulfonatos, los tensioactivos Sodium cocoyl isethionate y Sodium cocoyl glycinate han sido considerado suaves, así como el tensioactivo de Sodium lauroyl sarcosinate en el grupo de los carboxilados.10,11
Los tensioactivos anfóteros exhiben una carga variable, positiva o negativa, en la porción hidrofílica de la molécula, dependiendo del pH del medio en el que se encuentre: en pH alcalino, liberan un ion negativo (carga negativa); en pH ácido, liberan un ion positivo (carga positiva).12 Esta adaptabilidad hace que se utilicen junto con tensioactivos aniónicos o no iónicos para disminuir el tamaño de la micela. Aumentan la estabilidad de la espuma, detergencia y viscosidad, y su asociación promueve una formulación menos irritante para la piel.12
Químicamente, se agrupan en derivados de sulfobetaínas, aminoácidos, betaína (por ejemplo, Cocoamidopropyl betaine) e imidazolina (tal como Disodium cocoamphodiacetate). Estas dos últimas categorías son ampliamente empleadas en jabones y se consideran más suaves para la piel y los ojos que los tensioactivos aniónicos.12
En el tercer grupo de tensioactivos, los no iónicos no se disocian en iones en el agua, es decir, no tienen una carga positiva o negativa en la parte hidrofílica. Generalmente, derivan del óxido de etileno y/u óxido de propileno con un alcohol, y contienen un átomo de hidrógeno activo.13 Pero también se encuentran otros tipos, como alquilfenoles, ésteres de azúcar, alcanolamidas, óxidos de amina, ácidos grasos, aminas grasas, y polioles.13 Tienen la capacidad de estabilizar sus micelas (grupos de tensioactivos) y aumentar su suavidad. Algunos ejemplos son Polyethylene glycol (PEG)–80 Sorbitan laurate y Coco-glucoside.7
Recomendaciones internacionales y en América latina
Además de los tensioactivos, las formulaciones contienen otros ingredientes (fragancias, espesantes, antioxidantes, conservantes y colorantes) que pueden generar cambios en la barrera cutánea14,15 y desencadenar o agravar enfermedades dermatológicas, como dermatitis de contacto y dermatitis atópica.16 Las recomendaciones internacionales de asociaciones de profesionales de la salud y de consensos de expertos indican que la higiene del RN debe realizarse con productos suaves, preferiblemente líquidos, sin sustancias irritantes ni fragancias, y con un valor de pH entre ligeramente acidificado y neutro (5,5 a 7,0). Deben tener, además, prueba de impacto mínimo en el pH de la piel, seguridad oftálmica, y conservantes.14,17
En Brasil, el Ministerio de Salud recomienda que la limpieza de la piel neonatal se realice de manera suave, con material neutro, no tóxico y no abrasivo.18 Además, el consenso sobre el cuidado de la piel del RN recomienda el uso de jabón líquido que tenga un valor de pH más cercano al de la piel y con conservantes, para evitar la contaminación microbiana del producto y la piel del RN.19 Sin embargo, en Brasil, hay una gran variedad de productos de higiene para RN y niños disponibles en farmacias y mercados, en forma de jabón en barra o líquido, que no incluyen todas las recomendaciones mencionadas.
Los fabricantes de productos de higiene en Brasil cumplen con las regulaciones de la Agencia Nacional de Vigilancia Sanitaria (ANVISA), que define y clasifica los jabones para niños como grado de riesgo 1 exentos de registro sanitario.20,21 Es decir, son considerados de bajo riesgo para la población infantil, y no requieren de registro sanitario para su comercialización (solamente la notificación y envío de los documentos sobre los requisitos técnicos del producto por medio del sistema electrónico de la ANVISA).21
El reglamento también establece que deben estar compuestos por ingredientes propios y seguros, incluidos colorantes,22 conservantes23 y fragancias permitidas.24 Específicamente, para jabones en barra, aconseja que deben tener una alcalinidad libre y máxima de 0,5%.25 Sin embargo, no proporciona orientaciones sobre el valor de pH requerido para cada formulación. La regulación no obliga a poner en los rótulos información sobre el valor de pH, la proporción de los ingredientes o su función. Sólo es necesario mencionar los componentes detallados en la International Nomenclature of Cosmetics Ingredients (INCI),26 nomenclatura reconocida en el mundo para estandarizar ingredientes en rótulos de productos.
Adicionalmente, las empresas fabricantes de productos de higiene pueden realizar estudios de aceptabilidad en voluntarios bajo condiciones reales de uso para detectar irritación o alteraciones dermatológicas. Según el especialista que acompañe el estudio, el fabricante podrá colocar en el rótulo del producto los siguientes atributos:27
- Dermatológicamente probado, evaluado en humanos bajo control de un dermatólogo
- Oftalmológicamente probado, evaluado en humanos bajo el control de un oftalmólogo, con o sin dermatólogo
- Clínicamente probado, evaluado en humanos bajo el control de un dermatólogo u otro especialista, de acuerdo con el propósito del producto
- Evaluado por pediatras, evaluado en humanos (niños) bajo el control de un pediatra, acompañado o no por un dermatólogo, siempre que el producto haya sido previamente aprobado en las pruebas de seguridad realizadas en adultos
- Hipoalergénico, evaluado bajo el control de un dermatólogo o alergólogo, lo que demuestra una baja capacidad para inducir sensibilización (un proceso inflamatorio que involucra mecanismos inmunológicos, y que varía de días a años).
Por las implicaciones éticas, tales estudios no siempre se llevan a cabo en la población a la que están destinados (en este caso, RN). Todas las pruebas de seguridad se realizan en adultos sanos. Después de probar la seguridad de los productos, estos pueden someterse a pruebas con niños en condiciones normales de uso, bajo la supervisión del pediatra y respetando las pautas del comité de ética y los intereses del fabricante.
Por otro lado, los padres y cuidadores del RN se enfrentan a una amplia variedad de productos comerciales e ingredientes complejos que, la mayoría de las veces, desconocen. Esto dificulta la elección adecuada del producto.
El siguiente estudio busca ofrecer herramientas a los cuidadores y profesionales de la salud para la selección de productos de higiene, además de constituir una fase de análisis preliminar para respaldar la elección de dos jabones que formarán parte de un ensayo clínico aleatorio para evaluar el efecto del uso de estos productos en la piel del RN.
Método
Estudio cuantitativo y descriptivo, que analizó 17 jabones en la higiene del RN (8 en barra y 9 líquidos), y cuyo objetivo fue estudiar la información del rótulo, características físicas (color y fragancia) y fisicoquímicas (valor de pH) de los jabones usados. Los jabones se seleccionaron de acuerdo con la preferencia de las madres, los cuidadores y los profesionales de la salud responsables del cuidado de los RN hospitalizados en el Hospital Universitário de la Universidade de São Paulo en San Pablo, Brasil, tras haber respondido una pregunta abierta sobre el jabón que preferían usar para el baño del RN. Los productos referidos fueron adquiridos con fondos de la investigadora principal, para evitar conflicto de intereses.
Los jabones fueron comprados en una farmacia en la región occidental de la ciudad de San Pablo, en julio de 2018. Luego, fueron analizados en el laboratorio de cosmetología de la universidad pública Universidade de São Paulo. Se seleccionaron productos de diferentes marcas (Johnson's baby, Huggies, Granado, Pom Pom, Luddy y Dove Baby), en sus formas líquidas y en barra, ya que fueron las más referidas por los cuidadores y profesionales de la salud en la región.
A partir de los rótulos de los productos, fue analizada la información sobre tensioactivos utilizados, pruebas de seguridad, y descripción del valor de pH. La clasificación del tensioactivo y su potencial de irritación se verificaron mediante la nomenclatura INCI,26 la información disponible en la página web del Cosmetic Ingredient Review (CIR)28 y del Prospector,29 y las bases de datos Current Nursing and Allied Health Literature (CINAHL), Web of Science, Scopus y PubMed. Las características físicas analizadas fueron el color y la intensidad de la fragancia. Para las características fisicoquímicas, se midió el valor de pH. Todos estos parámetros fueron evaluados en el laboratorio, con el apoyo de un auxiliar de investigación y de acuerdo con la orientación de un profesional de farmacia.
Color, fragancia y pH
Para evaluar el color de formulaciones líquidas y en barra, se vertió el producto en un vaso de precipitado y el auxiliar de investigación informó el color que percibió. Para analizar la fragancia del jabón, se le solicitó que se llevara el producto a la nariz para percibir la fragancia y, luego, la clasificara como suave, moderada o fuerte.
Para la lectura del valor de pH, se usó un medidor de pH digital de mesa (Digimed DM-22, Digicrom Analítica Ltda, São Paulo, Brasil), calibrado con solución tampón de pH 4,0 y 7,0. En el caso de los jabones líquidos, se usaron 40ml en un vaso de precipitado de 50ml, en el cual fue sumergido el electrodo del medidor de pH. La lectura del pH se realizó tres veces con cada producto. Para los jabones en barra, se pesó 1g y se mezcló en 100ml de agua destilada. Luego, se calentó el producto en una placa calefactora (IKA C-MAG HS 7, KA-Werke GmbH & Co. KG, Staufen, Alemania) a 37°C y sobre un agitador magnético, hasta que se completó la dispersión de la muestra. La preparación fue enfriada a temperatura ambiente y se realizó la lectura del valor de pH, de la misma manera que para los jabones líquidos.
Los datos se almacenaron en el programa Microsoft Excel y fueron analizaron con el programa R, versión 3.6.1 (Microsoft, Washington, EEUU). El análisis descriptivo de los datos se realizó presentando los valores de frecuencias absolutas y relativas para las variables categóricas; para las variables numéricas, se utilizaron medidas de tendencia central, como la media y la desviación estándar (DE). El estudio no fue enviado para aprobación por el Comité de Ética en Investigación porque no involucró humanos.
Resultados
De acuerdo con la información obtenida de los rótulos de los productos, la clasificación de los jabones fue: seis (35%) líquidos tradicionales, seis (35%) barras tradicionales, tres (18%) barras combinadas y dos (12%) líquidos combinados (Tabla 1). La información de los rótulos evaluó el tipo de tensioactivo y su potencial de irritación, las pruebas de seguridad, las características físicas (color aparente e intensidad de la fragancia), y las características fisicoquímicas (valor de pH).
Tabla 1: Características de los jabones según informaciones del rótulo, análisis en el laboratorio, páginas web especializadas y bases de datos29,30,31,32,33,34,35,36,37,38,39,40,41,42,43,44,45,46,47,48,49,50,51,52
| Productoa | Tensioactivo (INCI)a,b | Tipo de tensioactivob | Potencial de irritaciónb | Pruebas de seguridada | Color aparentec | Intensidad de la fraganciac | Promedio pH (DE)c |
|---|---|---|---|---|---|---|---|
| Jabón líquido tradicional | |||||||
| Jabón 1 | Cocamidopropyl betaine | AF | B | HA | TL | S | 5,4 (0,2) |
| Coco-Glucoside | NI | B | DT | ||||
| Jabón 2 | Cocamidopropyl betaine | AF | B | HA | TL | M | 4,6 (0,0) |
| Coco-Glucoside | NI | B | DT | ||||
| Sodium Methyl 2-Sulfolaurate | AN | NR | |||||
| Disodium 2 Sulfolaurate | AN | NR | |||||
| Jabón 3d | Sodium laureth sulfate | AN | M | DT | A | S | 6,3 (0,0) |
| Decyl glucoside | NI | B | HA | ||||
| Cocamide dea | NI | M | |||||
| Tea-cocoyl glutamate | AN | NR | |||||
| Sodium stearate | AN | M | |||||
| Cocamidopropyl betaine | AF | B | |||||
| Jabón 4 | Sodium trideceth sulfate | AN | NR | HA | TL | F | 5,2 (0,0) |
| Cocamidopropyl betaine | AF | B | DT | ||||
| Disodium cocoamphodiacetate | AF | B | OT | ||||
| Sodium laureth - 13 carboxylate | AN | NR | |||||
| Jabón 5 | Disodium cocoamphodiacetate | AF | B | HA | VA | M | 5,0 (0,2) |
| Cocamidopropyl betaine | AF | B | DT | ||||
| Sodium lauroamphoacetate | AF | B | OT | ||||
| Disodium lauroamphodiacetate | AF | B | |||||
| Sodium laureth - 13 carboxylate | AN | NR | |||||
| Jabón 6 | Sodium laureth sulfate | AN | M | DT | TL | M | 7,4 (0,0) |
| Decyl glucoside | NI | B | OT | ||||
| Disodium cocoamphodiacetate | AF | B | |||||
| Sodium lauroyl sarcosinate | AN | B | |||||
| Jabón en barra tradicional | |||||||
| Jabón 7 | Sodium tallowate | AN | M | DT | Bg | M | 10,0 (0,1) |
| Sodium palm kernelate | AN | M | |||||
| Sodium Isethionate | AN | B | |||||
| Jabón 8 | Sodium tallowate | AN | M | DT | LC | M | 9,9 (0,1) |
| Sodium palm kernelate | AN | M | |||||
| Jabón 9 | Sodium tallowate | AN | M | DT | A | M | 10,1 (0,2) |
| Sodium palm kernelate | AN | M | |||||
| Jabón 10 | Decyl glucoside | NI | B | DT | Bg | F | 10,0 (0,1) |
| Sodium tallowate | AN | M | |||||
| Sodium palm kernelate | AN | M | |||||
| Jabón 11 | Sodium laureth sulfate | AN | M | DT | VC | M | 9,7 (0,1) |
| Jabón 12e | Sodium stearate | AN | M | NR | A | S | 10,0 (0,0) |
| Jabón en barra combinado (jabón tradicional y tensioativos sintéticos) | |||||||
| Jabón 13 | Sodium cocoyl isethionate | AN | B | HA | Bg | S | 5,0 (0,0) |
| Cocamidopropyl hydroxysultaine | AF | B | DT | ||||
| Jabón 14f | Sodium lauroyl isethionate | AN | B | OT | Bg | F | 7,3 (0,1) |
| Sodium isethionate | AF | B | DT | ||||
| Sodium stearate | AN | M | HA | ||||
| Sodium laurate | AN | M | EP | ||||
| Sodium palmate | AN | M | |||||
| Sodium oleate | AN | M | |||||
| Sodium myristate | AN | M | |||||
| Cocamidopropyl betaine | AF | B | |||||
| Jabón 15f | Sodium lauroyl isethionate | AN | B | OT | Bg | F | 7,4 (0,1) |
| Sodium isethionate | AF | B | DT | ||||
| Sodium stearate | AN | M | HA | ||||
| Sodium laurate | AN | M | EP | ||||
| Sodium palmate | AN | M | |||||
| Sodium oleate | AN | M | |||||
| Sodium myristate | AN | M | |||||
| Cocamidopropyl betaine | AF | B | |||||
| Jabón líquido combinado (jabón tradicional y tensioativos sintéticos) | |||||||
| Jabón 16f | Cocamidopropyl betaine | AF | B | OT | B | F | 7,0 (0,2) |
| Sodium cocoyl glycinate | AN | B | DT | ||||
| Sodium lauroyl isethionate | AN | B | EP | ||||
| Sodium tallowate | AN | M | |||||
| Sodium palm kernelate | AN | M | |||||
| Sodium cocoate | AN | M | |||||
| Sodium stearate | AN | M | |||||
| Sodium isethionate | AF | B | |||||
| Jabón 17f | Cocamidopropyl betaine | AF | B | OT | B | F | 7,2 (0,0) |
| Sodium cocoyl glycinate | AN | B | DT | ||||
| Sodium lauroyl isethionate | AN | B | EP | ||||
| Sodium tallowate | AN | M | |||||
| Sodium palm kernelate | AN | M | |||||
| Sodium cocoate | AN | M | |||||
| Sodium stearate | AN | M | |||||
| Sodium isethionate | AF | B | |||||
INCI: International Nomenclature of Cosmetics Ingredients. DE: desviación estándar. AF: anfótero. AN: aniónico. NI: no iónico. B: bajo. M: moderado. S: suave. F: fuerte. NR: no reportado. TL: translúcido. B: blanco. A: amarillo. VA: verde/amarillo. LC: naranja claro. VC: verde claro. HA: hipoalergénico. DT: dermatológicamente probado. OT: oftalmológicamente probado. EP: evaluado por pediatra.
a:información obtenida del rótulo.
b:información obtenida de las páginas web especializadas y bases de datos.
c:información obtenida en el laboratorio.
d:el rótulo describe que el producto tiene pH de la piel.
e:jabón usado en un hospital universitario de la ciudad de San Pablo.
f:el rótulo describe que el producto tiene pH neutro.
g:jabón sin colorantes (CI, por sus siglas en portugués) descritos en los ingredientes.
Tipo de tensioactivo y potencial de irritación
Se identificaron 27 tipos de tensioactivos: 70,3% (n=19) aniónicos, 18,5% (n=5) anfóteros, y 11,1% (n=3) no iónicos. Todos los jabones líquidos tradicionales y combinados presentaron dos o más tensioactivos en sucomposición. Los jabones en barra combinados (n=3) y las barras tradicionales (n=4) (100% y 67%, respectivamente) utilizaron dos o más tensioactivos en su composición. Sólo 33% (n=2) de los jabones en barra tradicionales contuvo un tipo de tensoactivo.
Los tensioactivos más presentes en los jabones líquidos tradicionales fueron Cocamidopropyl betaine (20%) y Disodium cocoamphodiacetate (12%); en los jabones en barra tradicionales, Sodium tallowate (33,3%) y Sodium palm kernelate (33.3%); en los jabones líquidos combinados, Cocamidopropyl betaine (14,3%), Sodium cocoate (14,3%), Sodium cocoyl glycinate (14,3%), Sodium isethionate (14,3%), Sodium palm kernelate (14,3%), Sodium stearate (14,3%), Sodium tallowate (14,3%), y Sodium lauroyl isethionate (14,3%), y, en los jabones en barra combinados, Cocamidopropyl betaine (11,1%), Sodium isethionate (11,1%), Sodium laurate (11,1%), Sodium lauroyl isethionate (11,1%), Sodium myristate (11,1%), Sodium oleate (11,1%), Sodium palm kernelate (11,1%), y Sodium stearate (11,1%) (Tabla 1). La mayoría fue de tipo aniónico (80%) y con potencial de irritación bajo y moderado.
El Cuadro 1 indica que el jabón en barra tradicional fue el producto que más utilizó tensioactivos aniónicos en su formulación (91,6%), seguido de los jabones en barra combinados (83,3%). Adicionalmente, los no iónicos fueron los tensioactivos con menor porcentaje de uso en las formulaciones de los jabones líquidos (20%) y en barra tradicionales (8,3%), y estuvieron ausentes en los jabones líquidos y en barra combinados.
Cuadro 1. Características de los tensioactivos más frecuentes en los jabones analizados
| Tensioactivos | Características químicas | Efecto potencial en la piel |
|---|---|---|
| Cocamidopropyl betaine53 |
|
|
| Sodium stearate54 |
|
|
| Disodium cocoamphodiacetate55 |
|
|
| Sodium tallowate54 |
|
|
| Sodium palm kernelate50 |
|
|
| Sodium lauroyl isethionate51 |
|
|
De los 27 tipos de tensioactivos encontrados en las formulaciones, 44,4% (n=12) podrían tener potencial de irritación bajo. Entre ellos, 41,6% (n=5) fueron aniónicos, 41,6% (n=5) anfóteros y 16,6% (n=2) no iónicos (Tabla 1). También, 37% (n=10) de los tensioactivos podrían tener potencial de irritación moderado, de los cuales 90% (n=9) fueron aniónicos y 10% (n=1), no iónicos. No se encontró información en las páginas web especializadas y en las bases de datos de 18,5% (n=5) de los tensioactivos presentes en las formulaciones. El jabón en barra tradicional fue el producto que presentó un porcentaje mayor de tensioactivos clasificados con posible potencial de irritación moderado (83,3%), seguido de los jabones líquidos combinados (83,3%). Además, los jabones líquidos tradicionales presentaron un porcentaje mayor de tensioactivos con posible potencial de irritación bajo (62,5%) seguido de los jabones en barra combinados (44,4%) (Tabla 2).
Tabla 2. Frecuencia absoluta y relativa de los tipos de tensioactivos usados y su potencial de irritación, según el tipo de jabón
| Tipo de tensioactivo | Líquido tradicionaln=6 | Barra tradicionaln=6 | Líquido combinadon=2 | Barra combinadon=3 | |||||
|---|---|---|---|---|---|---|---|---|---|
| n | % | n | % | n | % | n | % | ||
| Aniónico | 10 | 40 | 11 | 91,6 | 12 | 85,7 | 15 | 83,3 | |
| Anfótero | 10 | 40 | 0 | 0 | 2 | 14,2 | 3 | 16,6 | |
| No iónico | 5 | 20 | 1 | 8,3 | 0 | 0 | 0 | 0 | |
| Total | 25 | 100 | 12 | 100 | 14 | 100 | 18 | 100 | |
| Posible potencial de irritación | Líquido tradicionaln=6 | Barra tradicionaln=6 | Líquido combinadon=2 | Barra combinadon=3 | |||||
| n | % | n | % | n | % | n | % | ||
| Bajo | 15 | 62.5 | 2 | 16.6 | 6 | 42.8 | 8 | 44.4 | |
| Moderado | 4 | 16.6 | 10 | 83.3 | 8 | 57.1 | 10 | 55.5 | |
| No reportado | 5 | 20.8 | 0 | 0 | 0 | 0 | 0 | 0 | |
| Total | 24 | 100 | 12 | 100 | 14 | 100 | 18 | 100 | |
Pruebas de seguridad
Fueron identificados cuatro tipos de pruebas de seguridad citados en los rótulos de las formulaciones: dermatológicamente probado, hipoalergénico, oftalmológicamente probado, y evaluado por pediatras.
El 94,1% (n=16) de los jabones que citaron ser “dermatológicamente probados” fueron líquidos y en barra tradicionales y combinados; 47% (n=8) de los que citaron ser “hipoalergénicos” fueron líquidos tradicionales y en barra combinados; 42% (n=7) de los que indicaron ser “oftalmológicamente probados” fueron líquidos tradicionales y en barra combinados; y 23,5% (n=4) de los que se presentaron como “evaluados por pediatras” fueron en barra y líquidos combinados. Un 5,8% (n=1) de las formulaciones evaluadas no citó ningún tipo de prueba en el rótulo.
Características físicas: color aparente e intensidad de la fragancia
En cuanto al color, el 41,1% (n=7) fue blanco, presente en los jabones en barra tradicional y barra combinada; 23,5% (n=4) translúcido, en los jabones líquidos tradicionales; 17,6% (n=3) amarillo, en aquellos líquidos y barra tradicional; 5,8% (n=1) verde claro, encontrado en un jabón líquido tradicional; 5,8% (n=1) verde/amarillo, en una barra tradicional; y 5,8% (n=1) naranja claro, en una barra tradicional.
Todos los jabones tuvieron algún tipo de fragancia: 35,3% (n=6) de intensidad fuerte, 41,1% (n=7) moderada y 23,5% (n=4) leve. Las tres categorías de intensidad se percibieron en los jabones líquidos y en barra tradicionales. Prevaleció la intensidad suave y fuerte en los jabones líquidos y en barra combinados.
Características fisicoquímicas: valor de pH
El valor de pH de todos los jabones varió de 4,6 (ácido) a 10,1 (básico). Siete (41,2%) tuvieron un pH entre 4,5 y 7,0, y 10 (58,8%) pH entre 7,1 y 10,1 (Tabla 1). En promedio, el valor de pH de los jabones líquidos tradicionales fue 5,6 (DE 0,0). Para barra tradicional, 9,94 (DE 0,81); 6,57 (DE 0,1) para barra combinada, y 7,1 (DE 0,0) para líquidos combinados (Figura 1).
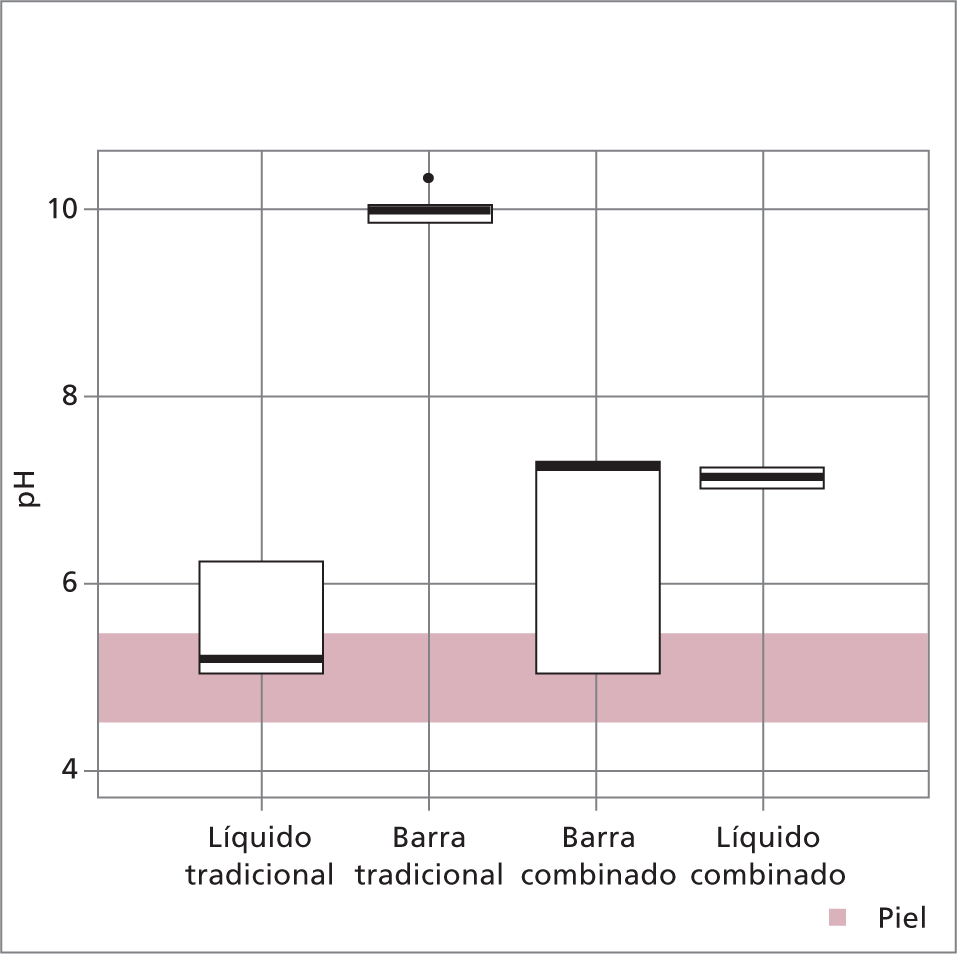
En el grupo de jabones líquidos tradicionales, cuatro (66,6%) estuvieron dentro del valor de pH de la piel (4,5 y 5,5). En los jabones en barra tradicionales, todos tuvieron un pH alcalino (entre 9,7 y 10,1). En los jabones en barra combinados, dos (66,6%) tuvieron un pH levemente alcalino (entre 7,3 y 7,4). Y, en el grupo de jabones líquidos combinados, todos (n=2) tuvieron un pH neutro y levemente alcalino (entre 7,0 y 7,2). Del total de jabones, cuatro (23,5%) describieron que el producto tenía un pH neutro sin proporcionar valores específicos. Sin embargo, al verificar sus valores de pH en el laboratorio, se encontró que uno tenía un pH de 7 (neutro) y los otros tres tenían un pH entre 7,2 y 7,4. Además, en el rótulo de un jabón líquido tradicional se describió que el producto tenía un pH fisiológico de la piel. No obstante, su valor de pH en el laboratorio fue de 6,3.
Discusión
Dependiendo de la composición química de cada tipo de tensioactivo, así como de las combinaciones de tensioactivos en un mismo producto, puede haber mayor o menor potencial de irritación sobre la piel.56 Los tensioactivos en forma de monómeros (individuales) o micelas (grupos de tensioactivos) pueden interactuar con los componentes del EC de manera no selectiva, es decir, no distinguen entre grasa, microorganismos y suciedad que se encuentran en la superficie de la piel y el EC.7,57 De esa manera, pueden interactuar con los lípidos epidérmicos, proteínas, células y neuroreceptores del EC.4,56
En el caso de los lípidos epidérmicos, los tensioactivos pueden emulsionar, desestabilizar y dañar la bicapa lipídica de los corneocitos, junto con los NMF contenidos en ellos, y provocar un aumento en la permeabilidad del EC.4 En las proteínas, producen una ligación que causa su desnaturalización, que interrumpe los mecanismos de retención de agua y genera inflamación en el EC.4 Esta ligación también desnaturaliza las enzimas del EC, lo que genera una disminución en la maduración de lípidos y proteínas, alteración en la formación de la bicapa, descamación exacerbada, y aspereza de la piel.4 La extensión de la ligación entre las proteínas y el tensioactivo dependerá de la carga y el tamaño del grupo polar de la molécula.4 En las células, los tensioactivos pueden llegar hasta el estrato granular, espinoso y basal, lo cual puede romper su membrana celular y causar la liberación de mediadores proinflamatorios (interleucinas o factor de necrosis tumoral alfa).4 En los neuroreceptores, pueden estimular los nociceptores tipo C responsables de la transmisión de estímulos químicos; esto puede observarse cuando hay una penetración profunda del tensioactivo en las capas de la piel.4 Teniendo en cuenta las características de la piel del RN, las interacciones mencionadas pueden impactar los procesos de maduración del EC y constituir un factor de riesgo para desarrollar afectaciones dermatológicas.
En vista de los efectos de los tensioactivos previamente expuestos, algunas empresas agregan lípidos (ceramidas, ácidos grasos, colesterol o triglicéridos) en la formulación para reemplazar los que fueron destruidos durante la higiene.8 Sin embargo, existe controversia porque el tiempo de contacto del producto no es suficiente para que dichos lípidos penetren en el EC. Y, en caso de penetrar, lo mismo podría suceder con los tensioactivos, causando daños acelerados al EC.8 Otras empresas agregan polímeros hidrofóbicamente modificados a los tensioactivos, para formar estructuras más grandes que no pueden penetrar en el EC y generan una disminución en la concentración de micelas durante la higiene, lo que produce menor daño a las proteínas.8 En el caso de la piel de los RN, esta última alternativa puede ser una estrategia eficiente para disminuir el impacto sobre los componentes del EC e interferir en menor grado con el equilibrio de los procesos fisiológicos de la piel.
El valor de pH de los jabones es otro factor relevante en la irritación de la piel y el daño del EC. El impacto del pH del jabón sobre el pH de la piel está influenciado por los ingredientes del producto, especialmente por los tensioactivos.4 En el presente estudio, se observaron grandes diferencias en el valor de pH entre todas las formulaciones, especialmente en los jabones en barra tradicionales, que tenían un promedio mayor que 9,0, por los tensioactivos aniónicos tipo “jabón”. Las formulaciones que mostraron valores (promedio) más cercanos a los valores del pH de la piel del RN una vez que adquiere estabilidad (entre 4,5 y 5,5) fueron los jabones líquidos y en barra combinados. Los valores de pH de los jabones líquidos y en barra tradicionales fueron similares a los de resultados reportados en otros estudios brasileños. El más reciente58 analizó el valor de pH de los jabones infantiles en barra (n=47) y líquidos (n=20). En el grupo de jabones en barra, 45 (95,8%) tuvieron un pH> 8.0, y en el grupo de los líquidos, siete (35%) mostraron un pH entre 7,0 y 7,9, mientras que 13 (65%) tuvieron un pH entre 4,4 y 6,9. Otro estudio,59 publicado hace más de 20 años, analizó el valor de pH de jabones en barra (n=23) y líquidos (n=5). En las formulaciones en barra, 22 (95,7%) tuvieron un pH> 8,0; en líquidos, tres (60%) mostraron un pH entre 7,0 y 7,9. Estos resultados sugieren que la fabricación de los jabones líquidos ha mejorado en los últimos años. Situación contraria es observada en los jabones en barra tradicionales, que continúan siendo fabricados con pH alcalinos (excepto los jabones en barra combinados).
El rótulo de cinco formulaciones analizadas presentó información cualitativa sobre el pH del producto, como “pH neutro” o “pH fisiológico de la piel”, sin proporcionar valores de pH específicos según la reglamentación vigente para estos productos. Al contrastar esta información con la lectura del valor de pH en el laboratorio, se observaron valores mayores de pH diferentes a lo referido en el rótulo. Tarun et al.60 encontraron resultados similares, ya que el 17% (n=11) de los 64 jabones para baño analizados tenía valores de pH diferentes de las descripciones encontradas en los rótulos, como “pH neutro” y “pH equilibrado”. Consideramos que este tipo de información no es clara para la población general, pues no se especifica el valor de pH del producto, el pH fisiológico de la piel ni la influencia que tendría la formulación sobre la homeostasis del funcionamento y estructura de la piel así como sobre la colonización por bacterias y virus, entre otros.
El uso de jabones con pH neutro a alcalino en la higiene diaria de adultos ha mostrado aumentar el valor de pH de la piel hasta en 3,0 unidades, que demora varias horas en recuperarse.4 Además, pueden ser observados cambios en la función de barrera, cohesión e integridad del EC, además de la recuperación y exfoliación celular, reducción de la microbiota residente y aumento de la colonización por microorganismos patógenos.61,62 La piel puede mostrar signos clínicamente visibles como resequedad, tensión, descamación, aspereza, eritema, prurito e inflamación de bajo grado.4,61,62 La piel puede reequilibrar los valores de pH dentro de lo fisiológico,58 pero se desconocen si estos efectos son producidos en la misma magnitud en la piel del RN.
Los estudios que evalúan los cambios y el tiempo de recuperación de los valores de pH de la piel después de la exposición a los jabones en los RN aún son limitados. El estudio de Gfatter et al.63 midió el pH de la piel de niños de dos semanas y 16 meses antes y después de 10 minutos de baño con tres formulaciones diferentes. En el grupo que usó jabón alcalino (pH=9,5) se dio el mayor cambio, con 0.453 unidades; en el grupo que usó syndet de barra (pH=5,5) y syndet líquido (pH=5,5) hubo un ligero aumento, con 0,294 y 0,291 unidades, respectivamente. El estudio no evaluó el tiempo de recuperación del pH de la piel.
De acuerdo con las implicaciones fisiológicas que las formulaciones con diferentes valores de pH pueden tener en la piel, algunos autores recomiendan el uso de productos ligeramente acidificados, es decir, con un valor de pH entre 4,0 y 5,0.4 Sin embargo, Blaak4,62 recomienda el uso de productos con un pH de 4,0 en poblaciones con una función de barrera afectada o inmadura, como es el caso de los RN, con o sin antecedentes de trastornos dermatológicos, como la dermatitis atópica. Así, los jabones líquidos tradicionales y en barra combinados serían los más adecuados en la higiene diaria de la piel del RN, para preservar su fisiología cutánea.
Otro aspecto relevante en las formulaciones es la seguridad ocular. En nuestro estudio, sólo 42% (n=7) de las formulaciones tuvo una descripción de seguridad oftálmica probada en el rótulo. Los productos con un pH más ácido (de 4,5 a 5,5), muy por debajo de la neutralidad (7,0), pueden causar irritación al entrar en contacto accidental con los ojos. Lo mismo ocurre con otros ingredientes de la formulación, como espesantes (Cocamide DEA) y conservantes (Methylclhoro). Además, en el RN, la respuesta defensiva del ojo (reflejo corneal) a un estímulo es mucho más lenta que en adultos hasta el cuarto mes de vida.17 Por lo tanto, la prueba de seguridad ocular de una formulación para RN debe ser un parámetro obligatorio que determine la elección de los padres y cuidadores.16
En Brasil, se perciben algunas razones que influyen en la compra de un producto: precio, fragancia y facilidad de uso. En nuestra experiencia con cuidadores y profesionales de la salud que atienden las necesidades de los RN, observamos que el precio del producto es un factor importante al momento de la selección, ya que comprar jabones en barra tradicionales puede ser más económico que comprar jabones líquidos tradicionales o combinados. La Asociación Brasileña de la Industria de Higiene Personal, Perfumería y Cosmética (ABIPECH) muestra que los jabones en barra eran los productos más consumidos, seguidos por los jabones líquidos, entre 2012 y 2019.64,65 Sin embargo, como consecuencia de la pandemia del Covid-19, hubo una intensificación en el aumento de consumo de jabón líquido con disminución del jabón en barra en la población general. Por lo tanto, es posible que esta situación también haya cambiado las preferencias de los productos de higiene para RN.66
Algunos cuidadores también relataron que manipular un jabón en barra durante el baño es más fácil y práctico que el jabón líquido. Otros, prefieren productos que tengan una fragancia más intensa y un efecto duradero en la piel, un concepto asociado con una limpieza eficiente. Sin embargo, hay investigaciones en adultos y RN que muestran que el uso de fragancias en jabones puede causar problemas alérgicos y dermatitis de contacto con mayor frecuencia.16,67,68 Por esta razón, las empresas deben considerar la fragancia (perfume) de la formulación al evaluar las pruebas de seguridad. Asimismo, se observó el uso de colorantes en seis (35,3%) de las formulaciones, y siete (41,1%) emplearon pigmento (dióxido de titanio). Sin embargo, todavía no hay evidencia que demuestre efectos nocivos sobre la función de barrera de la piel o el desarrollo de irritación y alergia a estos ingredientes.
Para que los cuidadores y profesionales de la salud puedan identificar los mejores productos, es importante tener acceso explícito y claro a informaciones como tipo de tensioactivo (clasificación y potencial de irritación), porcentaje en la formulación y función de cada ingrediente, valor de pH, fragancia, y detalles de las pruebas de seguridad y ensayos clínicos realizados (tipo de estudio, población, tiempo, resultados). Esto también incentivaría a las empresas a mejorar sus formulaciones y evaluarlas en rigurosos ensayos clínicos que verifiquen la ausencia de reacciones dermatológicas y cambios fisiopatológicos en la piel del RN a largo plazo.69
Por otro lado, consideramos que los profesionales de la salud, principalmente los enfermeros, son fundamentales a la hora de proporcionar recomendaciones a los padres y cuidadores sobre los productos de higiene. También, pueden analizar la evidencia científica disponible, que pueda contribuir a mejorar la legislación actual sobre productos cosméticos para RN y actualizar las políticas nacionales para el cuidado neonatal.69
A pesar de no contar con evidencia científica sólida sobre el efecto de los jabones en la piel de esta población, existen consensos y recomendaciones de especialistas nacionales e internacionales, que recomiendan que la selección de un jabón para RN debe seguir los siguientes criterios: jabones con tensioactivos con bajo potencial de irritación, con un valor de pH cercano al pH de la piel (entre 4,5 y 5,5), con pruebas dermatológicas y de seguridad ocular, con conservantes (para evitar la contaminación del producto por microorganismos), sin fragancia y sin colorante.4,14,16,17,18,19
Limitaciones
No fue posible analizar todas las marcas de jabones usados en RN (por ejemplo, syndet en barra) y que están disponibles en el mercado brasileño, ya que fueron evaluados los más citados por cuidadores y profesionales de la salud. De igual manera, fueron evaluados aspectos puntuales de la composición de los jabones. Sería ideal incluir otros parámetros en los análisis, como el uso de preservativos y espesantes. Además, es importante aclarar que dentro de algunos jabones hay sustancias químicas, diferentes a los tensoactivos, que reaccionan con otras moléculas y originan un tensioactivo, pero estos no fueron citados para evitar colocar datos equivocados sobre las formulaciones, ya que sólo el fabricante puede establecer con detalle las reacciones químicas de la formulación. Otro aspecto relevante es que es posible que algunos jabones presenten variaciones en los componentes químicos de los jabones.
Conclusión
La información del rótulo de todas las formulaciones analizadas indicó el uso de tensioactivos con potencial de irritación bajo y moderado. Al medir el valor de pH, hubo algunos jabones líquidos y en barra combinados que mostraron valores de pH cercanos al de la piel. Sin embargo, todos los jabones en barra tradicionales mostraron un pH alcalino (pH> 9.0). Se observó que cinco formulaciones proporcionaron informaciones sobre el pH, donde citaron pH neutro o pH fisiológico, pero dicha información fue inconsistente con los valores de pH analizados en el laboratorio. Todas las formulaciones citaron “probado dermatológicamente”, pero hubo un gran número que no citó “probado oftalmológicamente”. Con relación a las características físicas y fisicoquímicas, se concluyó que la fragancia estuvo presente en todos los jabones, en diferentes niveles de intensidad. El colorante se observó en algunas formulaciones, sin evidencia del posible efecto de irritación o alergia.
Este fue un estudio pionero en el territorio brasileño, ya que hace un abordaje inicial sobre la importancia de la composición de los productos de higiene en RN, e incentiva futuras investigaciones que permitan explorar de manera más amplia estos aspectos. Sugerimos la realización de investigaciones que involucren a la industria farmacéutica para desarrollar formulaciones que no alteren la función de barrera de la piel, no interfieran con el pH fisiológico, y cuenten con pruebas de seguridad para los RN. En el entorno clínico, recomendamos realizar ensayos clínicos rigurosos que evalúen el efecto de las formulaciones en barra y líquidas sobre la estructura y función de la piel de los RN a largo plazo.

